美国食物药品治理局(FDA)的加快审批步伐是为了鼓动勉励制药公司开发医治严峻或者危和生命疾病等未被满意临床需要的新药而设立的。加快审批步伐包括快速通道、冲破性疗法、加快核准,以和优先审评。快速通道、冲破性疗法及优先审评是特定药物承认,而加快核准是药物审评核准路子。综合2017—2021年FDA核准的立异药,利用加快步伐的立异药年均占比均于60%以上,近三年利用加快核准路子核准的立异药比例更是逐年上升。美国FDA的加快审批步伐鼓动勉励了新药开发者的踊跃性,特别鞭策了稀有病药物及临床急需药物的开发进程。
切合加快审批步伐的首要前提是于研药物所医治的疾病属在严峻疾病或者者严峻危和生命的疾病。得到优先审评、快速通道、冲破性疗法的药物均可以得到美国FDA提供的分外羁系引导或者者审批的优惠手续。这些优惠政策包括更多同FDA交流及会商的时机,或者于递交药物上市申请时答应资料滚动递交及审评等。除了了这些不异点,差别加快步伐有各自的特色及差别的要求(详见表)。
表 差别加快步伐的特色以和重要切合要求
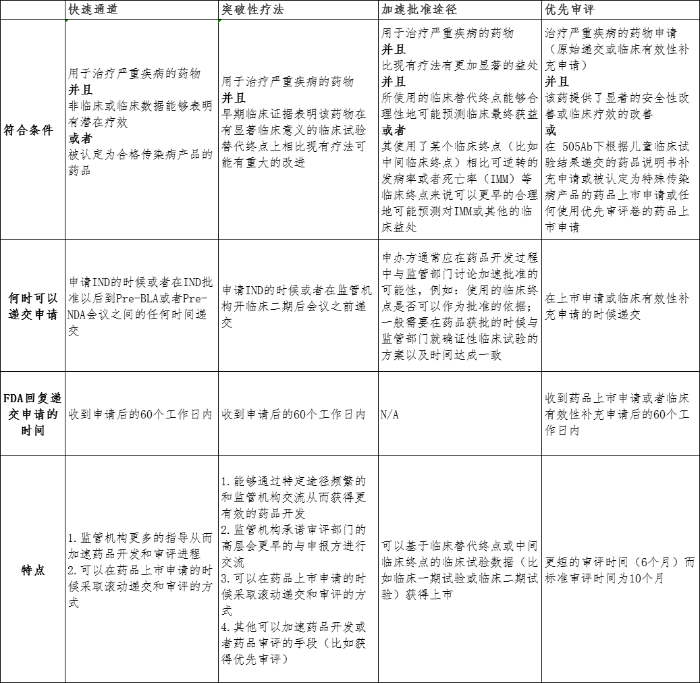
设立快速通道及冲破性疗法的目的是帮忙药物从开发快速推进到上市阶段,是以递交这些步伐的申请项目都是于临床实验申请(IND)阶段。但从切合前提来说,冲破性疗法的要求比快速通道更高,快速通道可以凭非临床数据就能够得到(注:属在非凡感染性疾病药物可以主动得到快速通道),而要想得到冲破性疗法认定,申报方必需至少于初期临床中就取患上有用性数据。申请快速通道,需要用证据注解于研药物对于未被满意的临床需求有潜于效果,这些撑持数据可以来自初期临床数据或者者仅仅来自在非临床数据(如来自药物于相干疾病模子上取患上的非临床有用性数据或者者可以或许撑持药物机理的非临床数据);有些于研药物于进入临床前或者者初期临床阶段可以依附非临床数据得到快速通道资历。而要切合冲破性疗法,则必需有充足的临床有用性数据,并且需要证实该研究药物比现有疗法有显著上风。虽然门坎更高,但得到冲破性疗法的药物所获得的优惠前提也会更多:除了与快速通道不异的便当前提外,一旦得到冲破性疗法认定,申报方还有可以获得更多来自美国FDA的引导及更多与FDA高层对于话的时机;此外于递交上市申请时,得到优先审批的概率也会增长。
优先审评重要是缩短药物递交上市申请后所需的审评时间,以是申请该资历的时间点是于递交上市申请或者者上市增补申请时。缩短审评时间,象征着于研药物可以或许更早举行贸易化或者早在竞争敌手举行贸易结构,这对于许多制药公司来讲是相称主要的。除了冲破性疗法药物许多时辰可以拿到优先审评资历外,还有有别的三个路子:关在儿童临床实验的增补申请;拿到非凡感染性疾病药物称呼的申请;利用优先审批卷。
以上特定药物承认或者者加快审评步伐其实不是排他性的,即一个药品可以同时得到多种特定药物承认。好比,一个药品可以于初期开发的时辰得到快速通道,以后跟着临床有用性数据的堆集得到冲破性疗法认定,然后于申请人及美国FDA告竣一致的环境下可以经由过程快速核准路子递交上市申请,末了于FDA审评时得到优先审评,固然这将是任何药品申办方求之不得的环境。
优先审评券是美国FDA最初为了激励热带疾病新药(包括生物成品)的研发,在2007年成立的一种优先审评券轨制。最早呈现于2007年美国《食物及药物治理局批改案法》(FDAAA),此中划定对于医治某些特定热带疾病的获批药物,颁布优先审评卷。美国国会或者FDA会按期更新切合前提的疾病类型。该卷的持有人可以将其用在该公司其他任何药物的上市申请,要求FDA赐与优先审评。此外,该卷持有人也能够将此卷让渡或者卖给其他制药公司。2012年,美国FDA安全及立异法案(FDASIA)划定了第二条得到优先审评卷的路子,即那些得到儿童稀有病药物称呼的药物于FDA核准后,也能够得到一张优先审评卷。2020年12月27日,美国国会决议于2026年9月30日以后住手儿童稀有病药物的优先审评卷轨制。FDA划定,优先审评卷只会于药物获批后颁给那些于2024年9月30日以前得到儿童稀有病药物称呼的药物。假如于2024年9月30日之后拿到儿童稀有病药物称呼,纵然于2026年9月30日以前得到核准,也没法拿到优先审评卷。
2016年,美国21世纪治愈法案(21st Century Cures Act)又增长了第三条可以得到优先审评卷的路子,即颁布优先审评卷给那些切合医疗对于策的医疗器械(好比小我私家防护用品)或者药品(好比一些非凡抗菌药或者疫苗等)。新冠病毒疫苗就满意上述前提,是以莫德纳的新冠病毒疫苗得到美国FDA核准上市后,还有得到了一张优先审评卷。2009年至2019年,FDA经由过程以上3种路子共颁布35张优先审评卷。
FDA答应优先审评卷的持有者生意业务此卷。结合医治公司曾经于2016年以3.5亿美元的高价将优先审评卷卖给艾伯维,后者将其用在乌帕替尼上市。近几年,该卷成交价基本于0.6亿~2亿美元之间。固然利用此卷并不是无任何危害或者价钱。FDA要求申报方于利用优先审评卷时,除了缴纳上市申请用度外,还有要再付出一笔分外的利用优先审评卷的用度。2022年,该用度约为120万美元。此外,FDA并不是每一次都能于6个月内完成优先审评。好比,日前FDA就将得到优先审评的传奇制药CAR-T疗法的审评时间延伸了4个月。及其他得到优先审评的申请同样,纵然利用优先审评卷得到优先审评,FDA也有可能延伸审评时间。
加快核准路子源在1992年,最初是为鼓动勉励艾滋病医治药物的开发,厥后逐步扩大到其他临床急需疾病医治药物。按照FDA网站数据,截至2021年6月30日,共有269个药品经由过程美国FDA加快核准路子获批上市。切合FDA加快核准的药物一般需要满意如下3个前提:医治严峻的、危和生命的疾病;核准所依据的临床数据基在替换临床尽头,且该替换尽头可能带到临床益处;所医治的疾病今朝缺乏有用的医治要领,或者者于研药物比现有尺度医治要领可以或许显著性提高临床疗效。也就是说,对于在那些临床未被满意需要的疾病,FDA为了尽快给患者带来新的疗法,愿意经由过程加快核准路子有前提地接管申报方因为基在替换尽头的临床实验数据所带来疗效的不确定性。
加快核准申报方需要于产物上市落伍行确证性临床实验以证实其临床效果。假如没有证实其临床效果或者申办方并无根据要求举行上市后确证性临床实验的,FDA可以保举或者要求申办方打消上市。固然,申报方可以上诉。
许多抗癌药物的上市都是基在以ORR或者PFS等临床替换尽头,或者者基在单臂临床实验数据,利用加快核准路子。以PD-(L)1免疫医治药物来讲,截至2021年6月,美国共核准7个PD-(L)1药物75个顺应症,此中35个顺应症的获批是经由过程加快核准路子。然而相称一部门药物于上市后没法于随后简直证性临床实验里证实疗效,是以加快核准路子饱受诟病。例如,上述35个获加快核准的PD-(L)1顺应症中,有31个举行了上市后简直证性临床实验,但只有9个乐成验证其临床效果,尚有4个验证掉败的申报方自动打消了上市申请。
据笔者统计,1992—2016年得到FDA加快核准的145个申请中,有111个申请终极得到彻底核准;有19个申请至今没有得到彻底核准;有15个申请终极由申报方打消。虽然年夜大都得到加快核准的药物终极得到了彻底核准,但还有是有相称一部门药物没有终极证实其疗效。此外,因为FDA并无明确或者同一要求申报方完成确证性实验的时间,是以许多申报方推延以致在索性不举行确证性临床实验。好比于1992-2016年加快核准的145个申请里,19个药品于上市平均9.5年后,仍旧没法提供有用的临床有用性数据或者没有举行确证性实验。许多人质疑加快核准路子匆匆地核准了药物,致使患者利用了没有充实颠末临床验证的“无效药物”;也有人责怪FDA没有和时打消那些没法于确证性实验里验证其临床疗效的药物,特别许多药物价格极其昂贵,是以呼吁FDA鼎新以致在打消加快审评路子的声音愈演愈烈。一些专家建议对于加快核准路子做出诸如增强对于上市后确证性临床研究的监控、提高FDA加快审评的透明性一致性等改良建议。笔者认为,虽然加快核准路子有些处所有待改善,但该轨制的实行确凿缩短了药物市场化的时间,而且年夜大都药物于加快核准后还有是证实了其疗效,这些药物特别是稀有病药物及缺少有用医治手腕的临床急需药物可以或许更早达到患者身旁。

每一周医药看点 (3月16日—22日)
国度医保局、国度成长鼎新委、国度卫生康健委结合发布《关在医保撑持下层医疗卫生办事成长的引导定见》,提出优化医保基金区域总额治理等14条举措,撑持下层医疗卫生办事成长;国度药监局决议将... 2026-03-24 16:50
每一周医药看点(3月9日—15日)
国度药监局发布通知布告,核准合肥立方制药株式会社的益气及胃胶囊为首家中药二级掩护品种;国度药监局发布《仿造药参比制剂目次(第一百零二批)》,包括复方氨基酸打针液(18AA-SF)等品种……... 2026-03-16 18:23-jinnianhui官网 - 金年会




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号